Heads up surgery
“Heads up surgery”とは術者が顕微鏡をのぞく代わりに、カメラで撮影された映像を3Dテレビで見ながら行う手術の事です。カメラで顕微鏡映像をデジタル化する事により、画面内に様々な追加情報を表示することができ、将来的に現在の顕微鏡手術より一歩進んだ手術が可能になるからです。現在、“Heads up surgery”を行える環境作りや、それに向けて4Kカメラを導入したらどうか?VRを導入したらどうか?どのような追加情報をどのように表示したらよいか?など一つずつ検証しています。将来的には今では想像もつかないような手術環境が作れるのではないかと考えています。
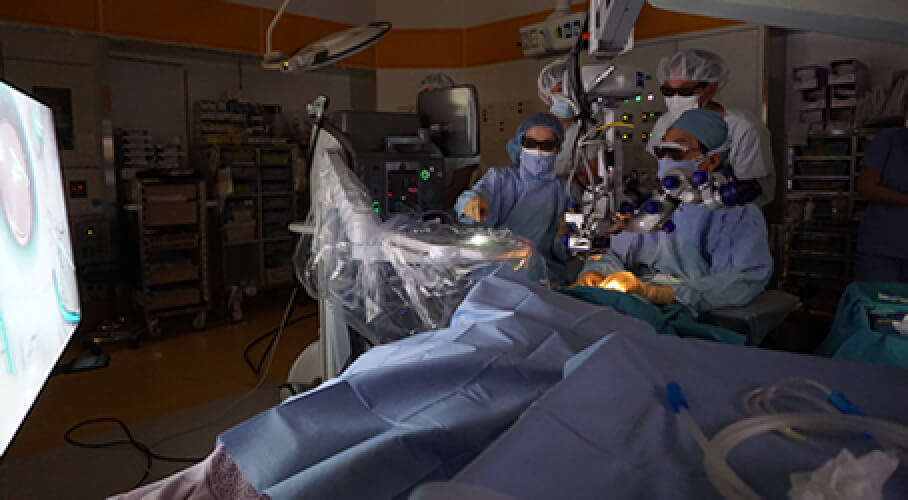
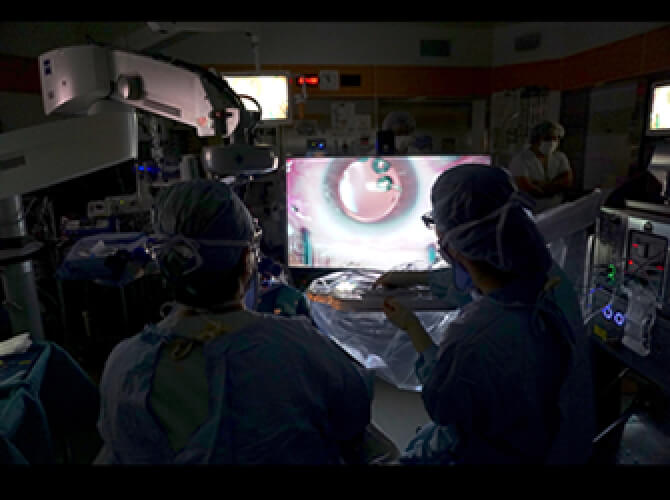
立体映像(3Dテレビ)
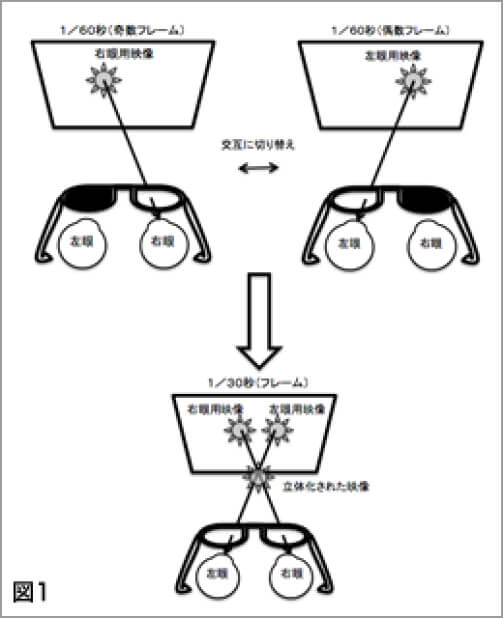
3D映画の「アバター」が公開された2009年以降、3D映画や3Dテレビが世間に普及し始めました。3D映像は右眼と左眼、それぞれ異なる映像を見せることで立体感を作り出す映像です(図1)。2D映像に比べ、臨場感が増すことや、奥行き感の情報が付加されることによる、リアルな映像になることが期待されています。
3D映画が世間に広まりだした頃、眼科手術映像の世界でも、画像のHD化と3D映像撮影のトライアルが始まりましたが、実用的な解像度や光量を得ることが難しく、“Heads up surgery”を行うことは、難しいという段階でした。
しかし技術進歩とともにカメラ性能は向上し、3Dテレビは低価格化が進み、2016年には複数社が3Dカメラ&テレビを用いた“Heads up surgery”の試作システムを開発しました。愛知医科大学では“Heads up surgery”を次世代の手術システム、またより良い手術教育システムとして導入するために、各社のシステムを比較検討しています。
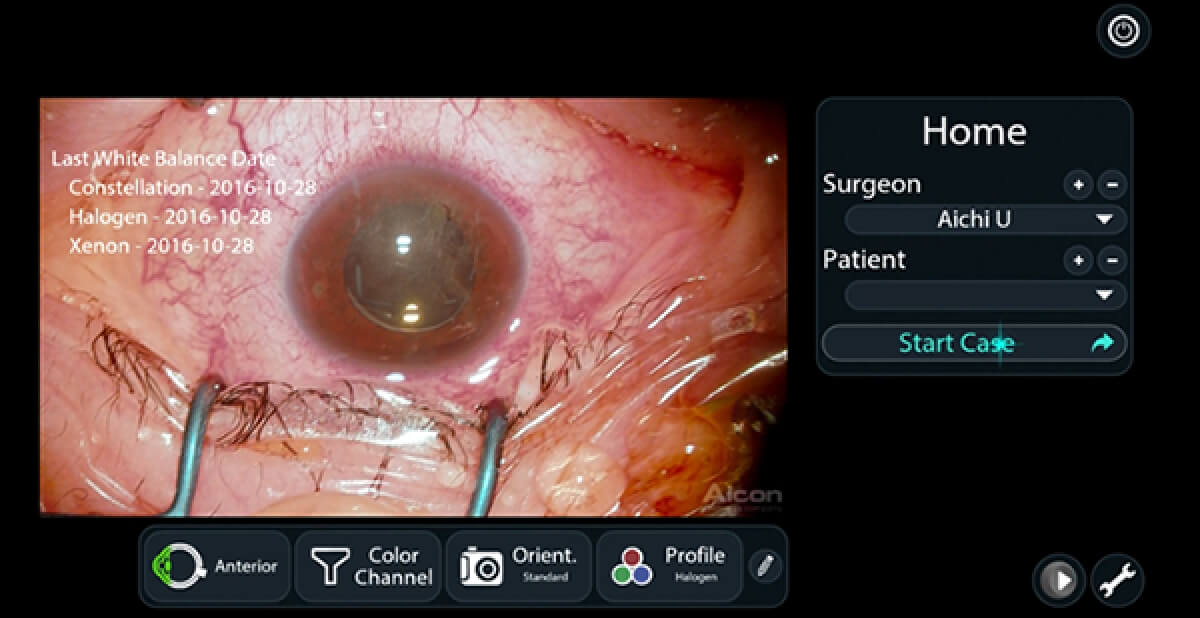
Heads up surgeryのメリット&デメリット
“Heads up surgery”を用いる利点の一つは、顕微鏡の鏡筒に縛られない自由な体勢で手術が行えることではないでしょうか?理科の実験や解剖で顕微鏡を覗いたことが有る方ならわかると思いますが、長時間の作業は疲労を生みます。もちろんこれまでは、長時間の手術も顕微鏡を覗きながら行ってきたわけですが、その姿勢は体に鞭打っての行為だったのです。“Heads up surgery”を用いると、顕微鏡に縛られず、自由な姿勢や向きで手術が行うことが出来ます。これは長時間の手術において、大きなメリットだと我々は考えており、モニターの位置、角度など、人間工学的に最適なものを模索しています。
またもう一つのメリットとして、術者と助手(及び見学者も)が同じ画面を共有できることです。同じ画面を見ることが出来ることで、これまでは伝わりにくかった術中の細かい注意点などが、言葉ではなく見ることで学ぶことが可能となります。これは助手だけではなく、見学者も同様であり、手術技術の向上に貢献すると思われます。
また従来の光源よりも暗くても明るく見ることができる点や、色を変更することにより硝子体の可視化を容易に行うことができるなど様々なメリットが考えられます。
一方、新しい技術でありコストがかかることや、見え方が変化することによる違和感、従来のやり方で十分ではないかなどの意見もあります。
しかし愛知医科大学では、この数年でのカメラ技術、3Dテレビの進歩を考え、デジタル技術が眼科手術領域に今後不可欠な要素になると確信しています。また手術教育においては、既存の技術では行えない術者の視点を共有することができており、今後その必要性はますます向上していくと考えています。
OCT Angiography
OCT Angiographyは光干渉断層計であるOCTを応用し、網膜の血流を造影剤無しで描出することを可能としています。この技術を用いることで、網膜血流の経時的変化や血流の層別解析が可能となり、網膜血流に関する新しい知見が得られることが期待されています。
OCT Angiographyの基本原理
OCT AngiographyはもともとドップラーOCTからの派生として開発されました。救急車のサイレンで有名なドップラー効果は、観測者から見て移動する物体が発する波の周波数が変化することで生じます。OCT Angiographyではこの移動する物=赤血球とすることで、網膜内の血流をOCTの信号から抽出することを可能としています。
OCT Angiographyの利点
OCT Angiographyの利点は、①非侵襲であること、②高解像度の画像が得られること、③層別に解析することができること、などがあります。
網膜血流評価ではフルオレセイン造影検査やインドシアニングリーン造影検査など、検査に造影剤が必要であるため、比較的侵襲の強い検査でした。
OCT Angiographyでは赤外光で撮影するのみですので、被検者の負担は軽くすみます。
またOCTの性能向上により、画像の解像度も良好なものが得られるようになっています。
そしてこれらの画像は3Dデータですので、網膜の層別に解析することが可能となり、これまでの造影検査では得られなかった治験が得られるようになっています。
当院での取り組み
当院ではOptovue社のAvanti XRとZeiss社のCirrus HD-5000を用いて、臨床的研究を行っております。

活性型プロテインC(APC:Activated Protein C)の
虚血網膜に対する効果検討
糖尿病網膜症や網膜静脈閉塞症に代表される網膜虚血性疾患は我が国における失明の主要原因となっています。現時点では、虚血網膜を間引くことで酸素の需給バランスを取る網膜光凝固が唯一の治療法でありますが、破壊的治療であり、根治療法ではありません。
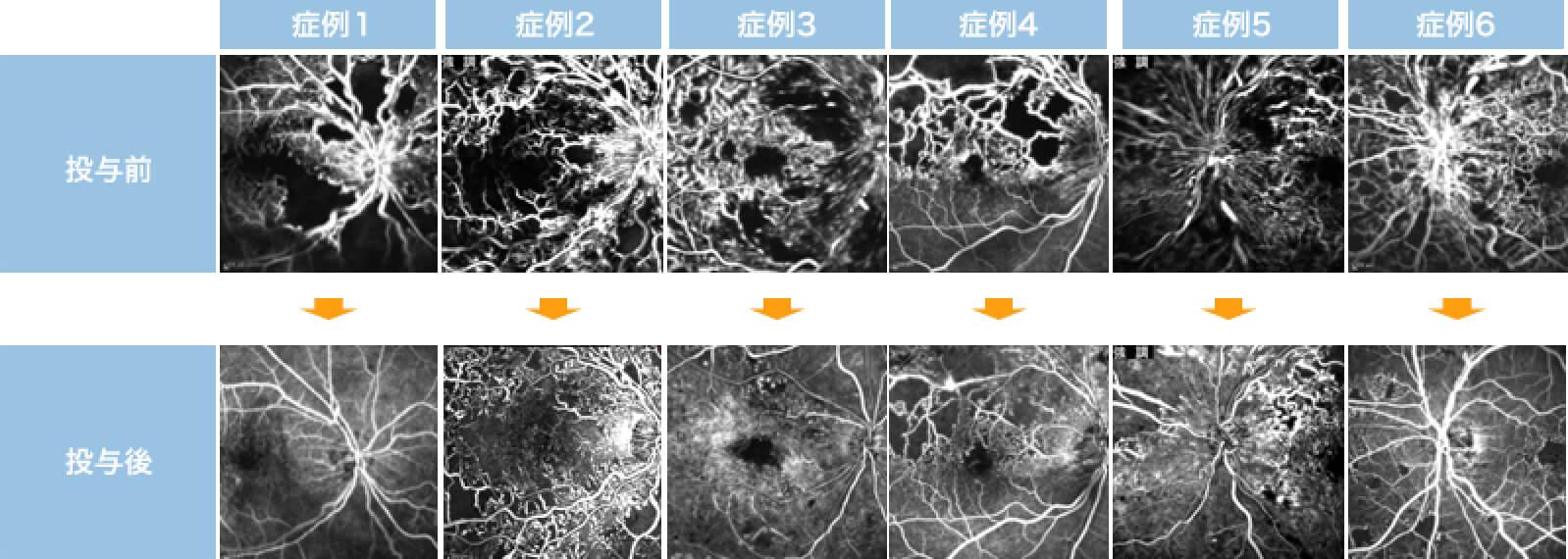
我々は活性型プロテインC(APC: Activated Protein C)の虚血網膜に対する効果を検討した結果、網膜細胞保護効果を見出しました(Invest Ophthalmol Vis Sci. 52:987, 2011)。そして、高度虚血型網膜中心静脈閉塞症を対象としたAPC眼内投与の医師主導型臨床試験の結果、広範囲の無灌流領域が再灌流する現象が、約6割の症例で見られました(図1、2)。広範囲の網膜血行再建に成功した世界初の報告となりました(JAMA Ophthalmol.132:361, 2014)が、再灌流の詳細なメカニズムは不明です。
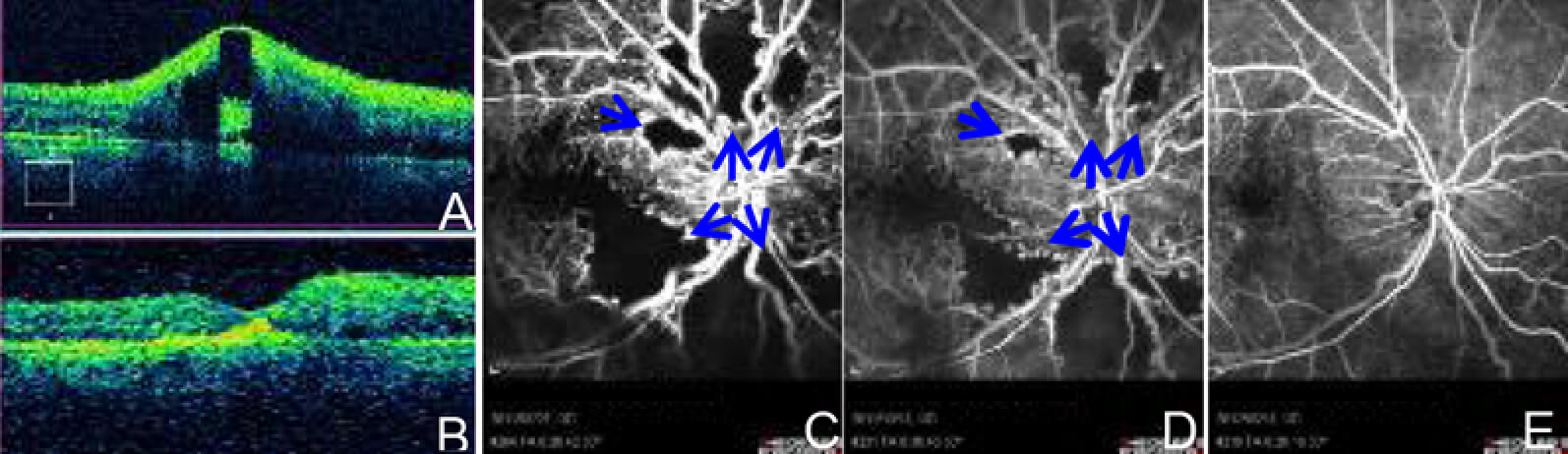
投与前(A)、および投与後1ヶ月(B)の網膜断層撮影。APC投与により網膜浮腫が完全に吸収されています。蛍光眼底造影(C-E)では、投与前(C)に見られた無灌流領域(矢印)が投与後3ヶ月(D)では面積比で58%減少し、投与後10か月(E)では完全に再灌流していました。
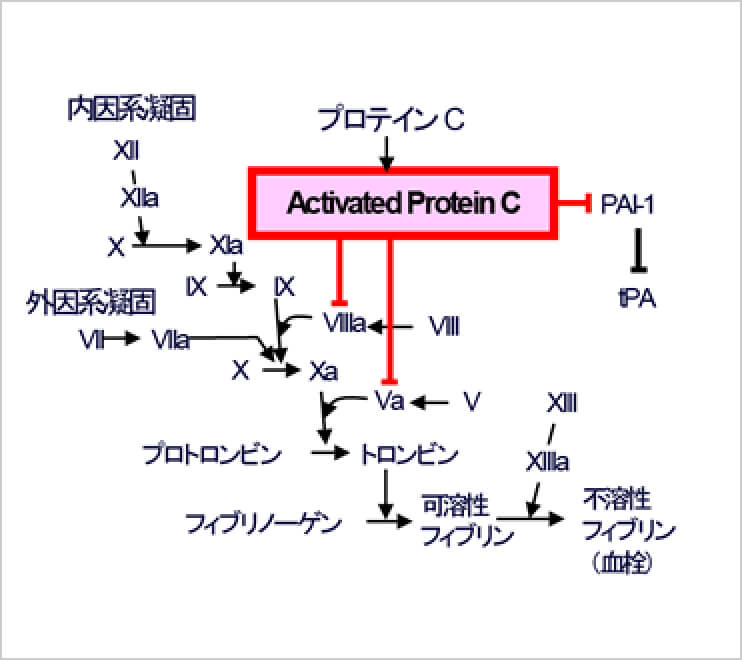
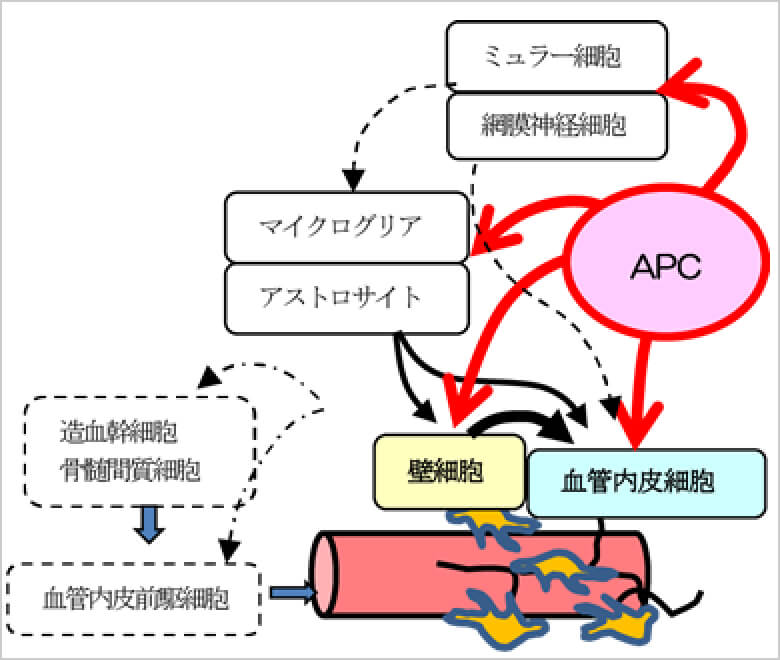
APCは本来、血液凝固制御因子であり、血栓形成抑制・線溶促進作用があります(図3)が、細胞保護作用・神経保護作用も有することが報告されています(Nat Med 9:338, 2003)。臨床で得られた再灌流には数カ月以上の時間がかかっていることから、血栓溶解に伴う短時間の再灌流作用ではなく、APCの持つ細胞保護効果や2次的な効果などにより1)新たな血管が形成されたり、あるいは、2)一旦消失した既存血管が再疎通した可能性が考えられます(図4)。臨床例での眼底造影写真からは、新たに形成された血管網と既存血管が吻合して灌流したのではないかと考えられる像が得られていますので、1)および2)の両方が緩徐に進行しているのではないかと言う仮説を立て、そのプロセスを、培養細胞/組織、および、動物実験で捉えることを目指します。
我々は、再灌流のメカニズムを培養細胞/組織を用いて解明し、有効な投与条件の開発や、全身の虚血性疾患への応用を目指しています。本研究は、広範囲の網膜再灌流に初めて成功したAPCによる薬物治療のメカニズムを解明する事を目指しており、現在難治とされている虚血性網膜疾患、ひいては、全身の虚血性疾患に対する根治療法を確立できる可能性があります。網膜症以外の糖尿病合併症や脳梗塞、心筋梗塞などにまで応用できれば、その社会的意義はきわめて大きいと考えています。